Адреналин
| Адреналин | |
|---|---|
| Epinephrine | |
 | |
 | |
 | |
| Химическое соединение | |
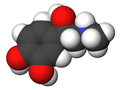
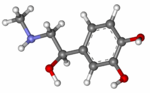
| ИЮПАК | (R)-4-[1-гидрокси-2-(метиламино)этил]-бензен-1,2-диол |
| Брутто-формула | C9H13NO3 |
| CAS | 51-43-4 |
| PubChem | 5816 |
| DrugBank | 00668 |
| Классификация | |
| Фармакол. группа | Адрено- и симпатомиметики (альфа-, бета-). Гипертензивные средства. |
| АТХ | A01AD01, B02BC09, C01CA24, R01AA14, R03AA01, S01EA01 |
| МКБ-10 | E16.2, H40.1, J45., R57., T78.2, T79.4, T81.1 |
| Лекарственные формы | |
| гранулы гомеопатические; капли для приёма внутрь гомеопатические; раствор 1 мг/мл, 1,8 мг/мл для инъекций; раствор 0,1 % для местного применения; раствор 1 % для наружного применения; субстанция-настойка гомеопатическая; субстанция-порошок | |
| Другие названия | |
| адреналин, адреналин синтетический, адреналина гидротартрат, адреналина гидрохлорид, «Адреналина гидрохлорид-Виал», эпинефрина гидротартрат | |
Адреналин (эпинефрин) (L-1 (3,4-Диоксифенил)-2-метиламиноэтанол) — основной гормон мозгового вещества надпочечников, а также нейромедиатор. По химическому строению является катехоламином. Адреналин содержится в разных органах и тканях, в значительных количествах образуется в хромаффинной ткани, особенно в мозговом веществе надпочечников. Играет важную роль в физиологической реакции «бей или беги».
Синтетический адреналин используется в качестве лекарственного средства под наименованием «Эпинефрин» (МНН).
Содержание
История
Был открыт в 1901 году.
Физиологическая роль
Адреналин вырабатывается нейроэндокринными клетками мозгового вещества надпочечников и участвует в реализации состояния, при котором организм мобилизуется для устранения угрозы. Его секреция резко повышается при стрессовых состояниях, пограничных ситуациях, ощущении опасности, при тревоге, страхе, при травмах, ожогах и шоковых состояниях. Содержание адреналина в крови повышается, в том числе, и при усиленной мышечной работе. Действие адреналина связано с влиянием на α- и β-адренорецепторы и во многом совпадает с эффектами возбуждения симпатических нервных волокон. Он вызывает сужение сосудов органов брюшной полости, кожи и слизистых оболочек; в меньшей степени сужает сосуды скелетной мускулатуры, но расширяет сосуды головного мозга. Артериальное давление под действием адреналина повышается. Однако прессорный эффект адреналина выражен менее, чем у норадреналина в связи с возбуждением не только α1 и α2-адренорецепторов, но и β2-адренорецепторов сосудов (см. ниже). Изменения сердечной деятельности носят сложный характер: стимулируя β1-адренорецепторы сердца, адреналин способствует значительному усилению и учащению сердечных сокращений, облегчению атриовентрикулярной проводимости, повышению автоматизма сердечной мышцы, что может привести к возникновению аритмий. Однако из-за повышения артериального давления происходит возбуждение центра блуждающих нервов, оказывающих на сердце тормозящее влияние, может возникнуть преходящая рефлекторная брадикардия. На артериальное давление адреналин оказывает сложное влияние. В его действии выделяют 4 фазы (см схему):
- Сердечная, связанная с возбуждением β1-адренорецепторов и проявляющаяся повышением систолического артериального давления из-за увеличения сердечного выброса;
- Вагусная, связанная со стимуляцией барорецепторов дуги аорты и сонного клубочка повышенным систолическим выбросом. Это приводит к активации дорсального ядра блуждающего нерва и включает барорецепторный депрессорный рефлекс. Фаза характеризуется замедлением частоты сердечных сокращений (рефлекторная брадикардия) и временным прекращением подъёма артериального давления;
- Сосудистая прессорная, при которой периферические вазопрессорные эффекты адреналина «побеждают» вагусную фазу. Фаза связана со стимуляцией α1- и α2-адренорецепторов и проявляется дальнейшим повышением артериального давления. Следует отметить, что адреналин, возбуждая β1-адренорецепторы юкстагломерулярного аппарата нефронов почек, способствует повышению секреции ренина, активируя ренин-ангиотензин-альдостероновую систему, также ответственную за повышение артериального давления.
- Сосудистая депрессорная, зависящая от возбуждения β2-адренорецепторов сосудов и сопровождающаяся снижением артериального давления. Эти рецепторы дольше всех держат ответ на адреналин.
На гладкие мышцы адреналин оказывает разнонаправленное действие, зависящее от представленности в них разных типов адренорецепторов. За счёт стимуляции β2-адренорецепторов адреналин вызывает расслабление гладкой мускулатуры бронхов и кишечника, а, возбуждая α1-адренорецепторы радиальной мышцы радужной оболочки, адреналин расширяет зрачок.
Длительная стимуляция β2-адренорецепторов сопровождается усилением выведения K+ из клетки и может привести к гиперкалиемии.
Адреналин — катаболический гормон и влияет практически на все виды обмена веществ. Под его влиянием происходит повышение содержания глюкозы в крови и усиление тканевого обмена. Будучи контринсулярным гормоном и воздействуя на β2-адренорецепторы тканей и печени, адреналин усиливает глюконеогенез и гликогенолиз, тормозит синтез гликогена в печени и скелетных мышцах, усиливает захват и утилизацию глюкозы тканями, повышая активность гликолитических ферментов. Также адреналин усиливает липолиз (распад жиров) и тормозит синтез жиров. Это обеспечивается его воздействием на β1-адренорецепторы жировой ткани. В высоких концентрациях адреналин усиливает катаболизм белков.
Имитируя эффекты стимуляции «трофических» симпатических нервных волокон, адреналин в умеренных концентрациях, не оказывающих чрезмерного катаболического воздействия, оказывает трофическое действие на миокард и скелетные мышцы. Адреналин улучшает функциональную способность скелетных мышц (особенно при утомлении). При продолжительном воздействии умеренных концентраций адреналина отмечается увеличение размеров (функциональная гипертрофия) миокарда и скелетных мышц. Предположительно этот эффект является одним из механизмов адаптации организма к длительному хроническому стрессу и повышенным физическим нагрузкам. Вместе с тем длительное воздействие высоких концентраций адреналина приводит к усиленному белковому катаболизму, уменьшению мышечной массы и силы, похудению и истощению. Это объясняет исхудание и истощение при дистрессе (стрессе, превышающем адаптационные возможности организма).
Адреналин оказывает стимулирующее воздействие на ЦНС, хотя и слабо проникает через гемато-энцефалический барьер. Он повышает уровень бодрствования, психическую энергию и активность, вызывает психическую мобилизацию, реакцию ориентировки и ощущение тревоги, беспокойства или напряжения. Адреналин генерируется при пограничных ситуациях.
Адреналин возбуждает область гипоталамуса, ответственную за синтез кортикотропин рилизинг гормона, активируя гипоталамо-гипофизарно-надпочечниковую систему и синтез адренокортикотропного гормона. Возникающее при этом повышение концентрации кортизола в крови усиливает действие адреналина на ткани и повышает устойчивость организма к стрессу и шоку.
Адреналин также оказывает выраженное противоаллергическое и противовоспалительное действие, тормозит высвобождение гистамина, серотонина, кининов, простагландинов, лейкотриенов и других медиаторов аллергии и воспаления из тучных клеток (мембраностабилизирующее действие), возбуждая находящиеся на них β2-адренорецепторы, понижает чувствительность тканей к этим веществам. Это, а также стимуляция β2-адренорецепторов бронхиол, устраняет их спазм и предотвращает развитие отёка слизистой оболочки. Адреналин вызывает повышение числа лейкоцитов в крови, частично за счёт выхода лейкоцитов из депо в селезёнке, частично за счёт перераспределения форменных элементов крови при спазме сосудов, частично за счёт выхода не полностью зрелых лейкоцитов из костномозгового депо. Одним из физиологических механизмов ограничения воспалительных и аллергических реакций является повышение секреции адреналина мозговым слоем надпочечников, происходящее при многих острых инфекциях, воспалительных процессах, аллергических реакциях. Противоаллергическое действие адреналина связано в том числе с его влиянием на синтез кортизола.
При интракавернозном введении уменьшает кровенаполнение пещеристых тел, действуя через α-адренорецепторы.
На свёртывающую систему крови адреналин оказывает стимулирующее действие. Он повышает число и функциональную активность тромбоцитов, что, наряду со спазмом мелких капилляров, обуславливает гемостатическое (кровоостанавливающее) действие адреналина. Одним из физиологических механизмов, способствующих гемостазу, является повышение концентрации адреналина в крови при кровопотере.
Фармакологическое действие
Фармакологические действия адреналина основывается на его физиологических свойствах (α,β-адреномиметик). В медицинской практике используются две соли адреналина: гидрохлорид и гидротартрат. Адреналин применяется в основном как сосудосуживающее, гипертензивное, бронхолитическое, гипергликемическое и противоаллергическое средство. Также назначается для улучшения сердечной проводимости при острых состояниях (инфаркт миокарда, миокардит и др.)
При скорости введения 0,04—0,1 мкг/кг/мин адреналин вызывает усиление и учащение сердечных сокращений, повышает ударный объём кровотока и минутный объём кровотока, уменьшает общее периферическое сосудистое сопротивление (ОПСС). В дозе выше 0,2 мкг/кг/мин адреналин суживает сосуды, повышает артериальное давление (преимущественно систолическое) и ОПСС. Прессорный эффект может вызвать кратковременную рефлекторную брадикардию. Расслабляет гладкие мышцы бронхов. Дозы выше 0,3 мкг/кг/мин уменьшают почечный кровоток, кровоснабжение внутренних органов, тонус и моторику желудочно-кишечного тракта.
Терапевтический эффект развивается практически мгновенно при внутривенном введении (продолжительность действия — 1—2 мин), через 5—10 минут после подкожного введения (максимальный эффект — через 20 минут), при внутримышечном введении — время начала эффекта вариабельное.
Способность суживать сосуды слизистых оболочек и кожи, замедлять кровоток используется в местной анестезии для снижения скорости всасывания анестетиков, что увеличивает продолжительность их действия и снижает системные токсические эффекты.
Фармакокинетика
При внутримышечном или подкожном введении всасывается непредсказуемо, так как оказывает непосредственное прессорное действие на капилляры в месте введения, существенно замедляющее поступление в системный кровоток и поэтому в экстренных случаях при невозможности внутривенного введения вводится интратрахеально или интракорпорально. Введение в мягкие ткани используется в виде обкалывания только с целью блокирования всасывания аллергизирующего вещества, введенного ранее и вызвавшего патологическую реакцию, при оказании помощи при анафилактическом шоке, иногда — для купирования капиллярных или паренхиматозных кровотечений. При внутривенном введении начинает действовать практически мгновенно. Также абсорбируется при эндотрахеальном и конъюнктивальном введении. Введенный парентерально, быстро разрушается. Проникает через плаценту, в грудное молоко, не проникает через гемато-энцефалический барьер.
Метаболизируется в основном МАО и КОМТ в окончаниях симпатических нервов и других тканей, а также в печени с образованием неактивных метаболитов. Период полувыведения при внутривенном введении — 1—2 мин.
Выводится почками в основном виде метаболитов: ванилилминдальной кислоты, метанефрина, сульфатов, глюкуронидов; а также в очень незначительном количестве — в неизменённом виде.
Применение
Показания
- Аллергические реакции немедленного типа (в том числе крапивница, ангионевротический шок, анафилактический шок), развивающиеся при применении лекарственных средств, сывороток, переливании крови, употреблении пищевых продуктов, укусах насекомых или введении др. аллергенов;
- бронхиальная астма (купирование приступа), бронхоспазм во время наркоза;
- асистолия (в том числе на фоне остро развившейся атриовентрикулярной блокады III ст.);
- кровотечение из поверхностных сосудов кожи и слизистых оболочек (в том числе из дёсен), артериальная гипотензия, не поддающаяся воздействию адекватных объёмов замещающих жидкостей (в том числе шок, травма, бактериемия, операции на открытом сердце, почечная недостаточность, хроническая сердечная недостаточность, передозировка лекарственных средств), необходимость удлинения действия местных анестетиков;
- гипогликемия (вследствие передозировки инсулина);
- открытоугольная глаукома, при хирургических операциях на глазах — отечность конъюнктивы (лечение), для расширения зрачка, внутриглазная гипертензия, остановка кровотечения; приапизм (лечение).
Противопоказания
- гиперчувствительность
- гипертрофическая кардиомиопатия
- феохромоцитома
- артериальная гипертензия
- тахиаритмия
- ишемическая болезнь сердца
- фибрилляция желудочков
- беременность
- период лактации.
С осторожностью
- метаболический ацидоз
- гиперкапния
- гипоксия
- фибрилляция предсердий
- желудочковая аритмия, легочная гипертензия
- гиповолемия
- инфаркт миокарда
- шок неаллергического генеза (в том числе кардиогенный, травматический, геморрагический)
- тиреотоксикоз
- окклюзионные заболевания сосудов (в том числе в анамнезе)
- артериальная эмболия
- атеросклероз
- болезнь Бюргера
- холодовая травма
- диабетический эндартериит
- болезнь Рейно
- церебральный атеросклероз
- закрытоугольная глаукома
- сахарный диабет
- болезнь Паркинсона
- судорожный синдром
- гипертрофия предстательной железы
- одновременное применение ингаляционных средств для общей анестезии (фторотана, циклопропана, хлороформа)
- пожилой возраст
- детский возраст.
Режим дозирования
Подкожно, внутримышечно, иногда внутривенно капельно.
- Анафилактический шок: в/в медленно 0.1—0.25 мг, разведенных в 10 мл 0,9 % раствора NaCl, при необходимости продолжают в/в капельное введение в концентрации 0.1 мг/мл. Когда состояние пациента допускает медленное действие (3—5 мин), предпочтительнее введение в/м (или п/к) 0.3—0.5 мг в разбавленном или неразбавленном виде, при необходимости повторное введение — через 10—20 мин (до 3 раз).
- Бронхиальная астма: п/к 0.3—0.5 мг в разбавленном или неразбавленном виде, при необходимости повторные дозы можно вводить через каждые 20 мин (до 3 раз), или в/в по 0.1—0.25 мг в разбавленном в концентрации 0.1 мг/мл.
- В качестве сосудосуживающего средства вводят в/в капельно со скоростью 1 мкг/мин (с возможным увеличением до 2—10 мкг/мин).
- Для удлинения действия местных анестетиков: в концентрации 5 мкг/мл (доза зависит от вида используемого анестетика), для спинномозговой анестезии — 0.2—0.4 мг.
- При асистолии: внутрисердечно 0.5 мг (разбавляют 10 мл 0,9 % раствора NaCl или др. раствором), но внутрисердечный способ введения препаратов не используют по причинам часто возникающих осложнений; во время реанимационных мероприятий — по 1 мг (в разбавленном виде) в/в каждые 3—5 мин. Если пациент интубирован, возможна эндотрахеальная инстилляция — оптимальные дозы не установлены, должны в 2—2.5 раза превышать дозы для в/в введения. Так же при проведении реанимационных мероприятий используют внутрикостный метод введения адреналина;
- Новорожденные (асистолия): в/в, 10—30 мкг/кг каждые 3—5 мин, медленно. Детям, старше 1 мес: в/в, 10 мкг/кг (в последующем при необходимости каждые 3—5 мин вводят по 100 мкг/кг (после введения, по крайней мере, 2 стандартных доз можно каждые 5 мин использовать более высокие дозы — 200 мкг/кг). Возможно использование эндотрахеального введения.
- Детям при анафилактическом шоке: п/к или в/м — по 10 мкг/кг (максимально — до 0.3 мг), при необходимости введение этих доз повторяют через каждые 15 мин (до 3 раз).
- Детям при бронхоспазме: п/к 10 мкг/кг (максимально — до 0.3 мг), дозы при необходимости повторяют каждые 15 мин (до 3—4 раз) или каждые 4 ч.
- Местно: для остановки кровотечений в виде тампонов, смоченных раствором препарата.
- При открытоугольной глаукоме — по 1 кап 1—2 % раствора 2 раза в день.
Передозировка
Симптомы:
- чрезмерное повышение АД
- тахикардия, сменяющаяся брадикардией
- нарушения ритма (в том числе фибрилляция предсердий и желудочков)
- похолодание и бледность кожных покровов
- рвота
- головная боль
- метаболический ацидоз
- инфаркт миокарда
- черепно-мозговое кровоизлияние (особенно у пожилых пациентов)
- отёк лёгких
- смерть
Лечение:
- прекратить введение
- симптоматическая терапия — для снижения АД — альфа-адреноблокаторы (фентоламин)
- при аритмии — бета-адреноблокаторы (пропранолол)
Побочное действие
Сердечно-сосудистая система: менее часто — стенокардия, брадикардия или тахикардия, сердцебиение, повышение или снижение АД, при высоких дозах — желудочковые аритмии; редко — аритмия, боль в грудной клетке.
-
Нервная система:
- более часто:
- головная боль
- тревожное состояние
- тремор
- менее часто:
- головокружение
- нервозность
- усталость
- нарушение терморегуляции (похолодание или жар)
- психоневротические расстройства:
- психомоторное возбуждение
- дезориентация
- нарушение памяти
- агрессивное или паническое поведение
- шизофреноподобные расстройства
- паранойя
- нарушение сна
- мышечные подёргивания
- более часто:
-
Пищеварительная система:
- часто — тошнота, рвота
-
Мочевыводящая система:
- редко — затрудненное и болезненное мочеиспускание (при гиперплазии предстательной железы).
-
Местные реакции:
- боль или жжение в месте внутримышечной инъекции.
-
Аллергические реакции:
- ангионевротический отёк
- бронхоспазм
- кожная сыпь
- многоформная эритема
- Прочие:
- редко:
- гипокалиемия
- менее часто:
- повышенное потоотделение
- судороги, стягивание мышц
- сильная эрекция, затрудняющая мочеиспускание
- редко:
Взаимодействие
Ослабляет эффекты наркотических анальгетиков и снотворных лекарственных средств.
При применении одновременно с сердечными гликозидами, хинидином, трициклическими антидепрессантами, допамином, средствами для ингаляционного наркоза (хлороформ, энфлуран, галотан, изофлуран, метоксифлуран), кокаином возрастает риск развития аритмий (вместе применять следует крайне осторожно или вообще не применять); с другими симпатомиметическими средствами — усиление выраженности побочных эффектов со стороны сердечно-сосудистой системы; с антигипертензивными средствами (в том числе с диуретиками) — снижение их эффективности.
Одновременное назначение с ингибиторами моноаминооксидазы (включая фуразолидон, прокарбазин, селегилин) может вызвать внезапное и выраженное повышение артериального давления, гиперпиретический криз, головную боль, нарушения ритма сердца, рвоту; с нитратами — ослабление их терапевтического действия; с феноксибензамином — усиление гипотензивного эффекта и тахикардию; с фенитоином — внезапное снижение артериального давления и брадикардию (зависит от дозы и скорости введения); с препаратами гормонов щитовидной железы — взаимное усиление действия; с препаратами, удлиняющими Q-T-интервал (в том числе астемизолом, цизапридом, терфенадином), — удлинение Q-T-интервала; с диатризоатами, йоталамовой или йоксагловой кислотами — усиление нейротоксических эффектов; с алкалоидами спорыньи — усиление вазоконстрикторного эффекта (вплоть до выраженной ишемии и развития гангрены).
Снижает эффект инсулина и других гипогликемических препаратов.
Антидоты — блокаторы альфа- и бета-адренорецепторов.
Особые указания
При инфузии следует использовать прибор с измерительным приспособлением с целью регулирования скорости инфузии.
Инфузии следует проводить в крупную (лучше в центральную) вену.
Внутрисердечно вводится при асистолии, если др. способы недоступны, так как существует риск тампонады сердца и пневмоторакса.
В период лечения рекомендовано определение концентрации K+ в сыворотке крови, измерение АД, диуреза, МОК, ЭКГ, центрального венозного давления, давления в легочной артерии и давления заклинивания в легочных капиллярах.
Чрезмерные дозы при инфаркте миокарда могут усилить ишемию путём повышения потребности миокарда в кислороде.
Увеличивает гликемию, в связи с чем при сахарном диабете требуются более высокие дозы инсулина и производных сульфонилмочевины.
При эндотрахеальном введении всасывание и окончательная концентрация препарата в плазме могут быть непредсказуемы.
Введение эпинефрина при шоковых состояниях не заменяет переливания крови, плазмы, кровезамещающих жидкостей и/или солевых растворов.
Эпинефрин нецелесообразно применять длительно (сужение периферических сосудов, приводящее к возможному развитию некроза или гангрены).
Строго контролируемых исследований применения эпинефрина у беременных не проведено. Установлена статистически закономерная взаимосвязь появлений уродств и паховой грыжи у детей, матери которых применяли эпинефрин в течение I триместра или на протяжении всей беременности, сообщалось также в одном случае о возникновении аноксии у плода после в/в ведения матери эпинефрина. Эпинефрин не следует применять беременным при АД выше 130/80 мм рт. ст. Опыты на животных показали, что при введении в дозах, в 25 раз превышающих рекомендуемую дозу для человека, вызывает тератогенный эффект.
При применении в период кормления грудью следует оценивать риск и пользу вследствие высокой вероятности возникновения побочных эффектов у ребёнка.
Применение для коррекции гипотензии во время родов не рекомендуется, поскольку может задерживать вторую стадию родов; при введении в больших дозах для ослабления сокращения матки может вызвать длительную атонию матки с кровотечением.
Можно использовать у детей при остановке сердца, однако следует соблюдать осторожность, поскольку в схеме дозирования требуются 2 разные концентрации эпинефрина.
При прекращении лечения дозы следует уменьшать постепенно, так как внезапная отмена терапии может приводить к тяжелой гипотензии.
Легко разрушается щелочами и окисляющими средствами.
Если раствор приобрел розоватый или коричневый цвет или содержит осадок, его вводить нельзя. Неиспользованную часть следует уничтожать.

