H5N1
| Influenza A virus H5N1 | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
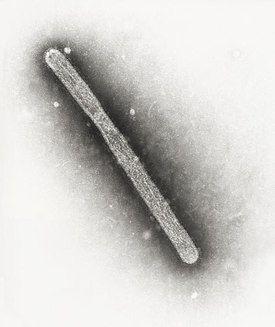 Вирион вируса гриппа H5N1 | |||||||||||||||||||||
| Научная классификация | |||||||||||||||||||||
|
промежуточные ранги
| |||||||||||||||||||||
| Международное научное название | |||||||||||||||||||||
|
Influenza A virus H5N1 | |||||||||||||||||||||
| Другие подтипы | |||||||||||||||||||||
| Группа по Балтимору | |||||||||||||||||||||
| |||||||||||||||||||||
H5N1 (HPAI A(H5N1), от англ. highly pathogenic avian influenza — высокопатогенный «птичий грипп») — подтип вируса гриппа A. Может вызвать заболевание как у людей, так и у многих других видов животных. С 2007 года заболевание, вызываемое одним из штаммов подтипа, приспособленным к птицам, стало широко известно под названием «птичий грипп».
Вирус — эндемик в большинстве птичьих популяций, особенно в Юго-Восточной Азии. Один из штаммов HPAI A(H5N1) распространяется по всему миру после первого появления в Азии. Этот штамм вызывает эпизоотию (эпидемия среди животных кроме человека), а затем и панзоотию (затронув животных множества видов на огромной территории), вызывая гибель десятков миллионов птиц. Чаще всего упоминания о «птичьем гриппе» и H5N1 относятся именно к этому штамму.
Содержание
Обзор
HPAI A(H5N1) — птичье заболевание. Существуют некоторые данные о частных случаях передачи HPAI A(H5N1) от человека человеку. Наибольший фактор риска заражения — контакт с заражёнными птицами, но передача вируса от птиц человеку малоэффективна.
В большинстве случаев те, кто заразился H5N1 находились в физическом контакте с птицами. Всё же, около 60 % известных случаев заражения людей современным азиатским штаммом HPAI A(H5N1) привели к их гибели, к тому же H5N1 может мутировать или реорганизоваться в штамм, способный передаваться от человека человеку. В 2003 году известный в мире вирусолог Роберт Вебстер опубликовал статью под названием «Мир качается на грани эпидемии, которая может уничтожить большую часть человеческой популяции» в журнале American Scientist. Он призвал к организации адекватных ресурсов для борьбы с тем, в чём он видел главную опасность для, возможно, миллиардов жизней. 29 Сентября 2005 года, Дэвид Набарро, недавно назначенный главным координатором по птичьему и человеческому гриппу Объединённых наций, предостерёг мир о том, что прорыв птичьего гриппа может уничтожить от 5 до 150 миллионов человек. Эксперты выделили ключевые события (создание новых клад, инфицирование новых видов, распространение в другие регионы), отмечая прогресс птичьего гриппа до размеров пандемии, и многие из тех ключевых моментов случились намного быстрее, чем ожидалось.
Из-за высокой летальности и вирулентности HPAI A(H5N1), его эпидемического проявления, большого и растущего множества носителей и значительных продолжающихся мутаций, H5N1 считается наиболее большой пандемической опасностью в наше время. Миллиарды долларов выделяются на его изучение и подготовку к возможной пандемии гриппа.
Как минимум 12 компаний и 17 правительств разрабатывают вакцины против гриппа в 28 клинических учреждениях, что, если удастся, может обернуть смертельную инфекцию в менее опасную. Как минимум три месяца понадобится для того, чтобы начать массовое производство вакцины, предотвращающей любые симптомы заболевания, после начала проявления вируса. Однако есть надежда, что в течение года после первого проявления вируса, появится возможность увеличить производство вакцины до миллиарда доз.
H5N1 может стать причиной более чем одной эпидемии гриппа, поскольку ожидают, что он будет продолжать мутировать в птицах независимо от выработанного в человеке иммунитета к штамму.
Эпидемия от генетических потомков гриппа может включать подтипы вируса гриппа А отличные от H5N1. В то время, как генетический анализ вируса H5N1 показывает, что эпидемии от его потомков могут быть более летальными, чем эпидемия Испанского гриппа, планирование борьбы с будущей пандемией основывается на всём, что может быть сделано при индексе опасности пандемии пятого уровня, который, грубо говоря, является самым высоким и соответствует угрозам степени испанского гриппа или ещё выше; для этого уровня предполагается использовать все возможные меры пресечения.
Генетика
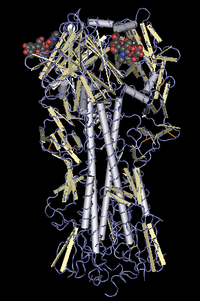
Первый обнаруженный штамм HPAI A(H5N1) (названным A/chicken/Scotland/59) стал причиной гибели двух стай кур в Шотландии в 1959 году; однако тот штамм отличался от высоко-патогенного штамма H5N1 наших дней. Доминирующий штамм HPAI A(H5N1) 2004 года эволюционировал с 1999 по 2002 год с образованием генотипа Z. Его так же назвали «Азиатская разновидность HPAI A(H5N1)».
Азиатские разновидности HPAI A(H5N1) разделены на две антигенные клады. "Клада 1 включает в себя отдельные человеческие и птичьи изоляты из Вьетнама, Таиланда, и Камбоджи и птичьи изоляты из Лаоса и Малайзии. Вирусы клады 2 были впервые найдены в группах птиц Китая, Индонезии, Японии и Южной Кореи до того, как они распространились на запад в Средний Восток, Европу и Африку. Именно вирусы клады 2 были изначально ответственны за заражения людей, которые впервые случились в конце 2005 года и в 2006 году, согласно ВОЗ. Генетический анализ выделил шесть подклассов клады 2, три из которых имеют определённое географическое распространение и связаны с инфицированием человека: Карта (недоступная ссылка). Архивировано 25 ноября 2006 года.
- Подкласс 1, Индонезия
- Подкласс 2, Европа, Средний Восток и Африка (названные ЕСА)
- Подкласс 3, Китай
Исследование от 2007 года, сфокусированное на подклассе ЕСА, пролило больше света на мутации ЕСА. «36 новых изолятов, зарегистрированных в регионе, значительно расширили данные последовательностей генома, ранее полученных из предыдущих изолятов птичьего гриппа (H5N1). До запуска нашего проекта в GenBank было только 5 других полных геномов из Европы за период 2004—2006 гг., без единого полного генома из Среднего Востока и северной Африки. Наш анализ позволил сделать несколько открытий. Во-первых, все Европейские, средневосточные и африканские образцы принадлежат кладе, которая обособлена от других азиатских клад, у которых есть признаки общего предка — оригинального Гонг-Конгского штамма 1997 года. Филогенетические деревья, построенные по каждому из 8-ми сегментов показывают последовательное родство 3-х групп, как показано на HA дереве на иллюстрации 1. Две клады содержат исключительно Вьетнамские изоляты; меньшая из клад, с 5-ю изолятами, отмечена как V1; большая клада, с 9-ю изолятами — V2. Оставшиеся 22 изолята отделены в третью, очевидно отличную, кладу, отмеченную как ЕСА, которая включает в себя образцы из Европы, Среднего Востока и Африки. Деревья для оставшихся 7-ми сегментов проявляют меньшую топологию с кладами V1, V2 и ЕСА, чётко отделённую в каждом случае. Исследования всех доступных полных геномов гриппа (H5N1), а также 589ти HA последовательностей показали, что ЕСА клада чётко отличается от большинства клад, циркулирующих в Китае, Индонезии и Юго-Восточной Азии.»
Терминология
Изоляты H5N1 определяются по примеру A(H5N1): A/курица/Накорн-Патом/Таиланд/CU-K2/04(H5N1):
- A означает серовар вируса (A, B или C).
- курица — вид, от которого был получен изолят.
- Накорн-Патом/Таиланд — место, в котором был найден вирус.
- CU-K2 дифференцирует от других изолятов, найденных в том же регионе.
- 04 означает, что изолят был впервые выделен в 2004 году.
- H5 означает, что суперкапсид вируса содержит пятый тип гемагглютинина из нескольких известных.
- N1 означает, что суперкапсид вируса содержит нейраминидазу первого из нескольких известных типов.
(Другие примеры: A/утка/Гонг Конг/308/78(H5N3), A/птица/NY/01(H5N2), A/курица/Мексика/31381-3/94(H5N2), and A/утка/Египет/03(H5N2)).
Так же как и другие вирусы гриппа, у H5N1 есть штаммы, названные «высокопатогенными» (ВП) и «низкопатогенными» (НП). Вирусы птичьего гриппа, вызвавшие HPAI (рус.: ВППГ — высоко-патогенный птичий грипп) — высоковирулентны, причём уровень смертности в инфицированных стаях достигает 100 %. LPAI (рус.: НППГ — низко-патогенный птичий грипп) вирусы обладают незначительной вирулентностью, однако могут быть прародителями HPAI вирусов. Текущий штамм H5N1, ответственный за смерть птиц по всему миру, является HPAI вирусом; все остальные штаммы H5N1 в наше время, включая Североамериканский штамм, который не вызывает заболевания вообще в любых видах животных и птиц, являются LPAI штаммами. Все, обнаруженные к настоящему времени HPAI штаммы затрагивают H5 и H7 подтипы. Эти различия/классификация касаются домашней птицы, а не человека. Обычно, высокопатогенные птичьи вирусы не являются ВП для человека или не-домашней птицы. Необычно, что современный HPAI штамм H5N1 смертелен для столь многих видов, включающих домашних кошек, которые никогда ранее не были восприимчимы к ни одному из вирусов гриппа.
Генетическая структура и родственные подтипы

H5N1 — это подтип вида Вирус гриппа А рода Influenzavirus A семейства Orthomyxoviridae. Как и все другие подтипы гриппа А, подтип H5N1 — РНК вирус. У него сегментированный геном восьми /негативный геном/ молекул одноцепочечной РНК с аббревиатурами PB2, PB1, PA, HA, NP, NA, MP и NS.
HA кодирует гемагглютинин, антигенный гликопротеин, найденный на поверхности вирусов гриппа ответственный за сцепление вируса с клеткой, которую он инфицирует. NA кодирует нейраминидазу, антигенный глюкозилированный (англ. glycosylated) энзим, ответственный за освобождение потомков вируса от инфицированных клеток.
Гемагглютининовые (HA) и нейраминидазные (NA) цепочки РНК определяют структуру белков практически идентичных тем, на которые нацелены большинство медицинских антивирусных препаратов и антибиотиков. На основаниее HA и NA также образуются названия различных вирусов гриппа A. Именно оттуда происходят H и N в названии H5N1.
Вирус гриппа А очень существенен из-за его огромного потенциала вызывать заболевания и смерть человека и других животных. Подтипы вируса гриппа А, вызвавшие пандемические смерти человека включают:
- H1N1 — вызвал испанский грипп (испанку) и в наше время вызывает сезонные заболевания гриппом, известен с 2009 года как «свиной грипп»
- H2N2 — азиатский грипп
- H3N2 — вызвал «гонгконгский» грипп и в наше время вызывает сезонные заболевания гриппом
- H5N1 — самая большая пандемическая опасность нашего времени
- H7N7 — обладает необычным зоонозным потенциалом; стал причиной смерти одного человека
- H1N2 — свойственен человеку и свиньям, вызывает сезонные заболевания/эпидемии гриппа у человека.
- H9N2 — инфицировал трёх человек
- H7N2 — инфицировал двух человек
- H7N3 — инфицировал двух человек
- H10N7 — инфицировал двух человек
Слабо-патогенный H5N1
Люди и H5N1
Симптомы у людей
Гемагглютинин птичего гриппа связывает рецепторы сиаловой кислоты альфа 2-3, в то время как хемагглютинин человеческого гриппа связывает рецепторы сиаловой кислоты альфа 2-6. Обычно имеются и другие отличия. Пока же не существует человеческой формы H5N1, поэтому все люди, заразившиеся вирусом, заразились птичьим H5N1.
В общем случае люди, заразившиеся адаптировавшимся к человеку вирусом гриппа А, обычно имели симптомы, включающие лихорадку, кашель, фарингит, мышечные боли, конъюнктивит и, в более тяжелых случаях, проблемы с дыханием и пневмонию с вероятностью смертельного исхода. Тяжесть заболевания в большинстве своём зависит от состояния иммунной системы больного и также от того, был ли он заражён штаммом до этого (в последнем случае человек практически невосприимчив к вирусу). Неизвестно будут ли эти или другие симптомы у гриппа H5N1 адаптированного к человеку.
Отчеты о высокопатогенном вирусе птичего гриппа H5N1 говорят о высокой смертности среди людей. Данные ВОЗ показывают, что 60 % случаев с диагнозом H5N1 были смертельны. Однако, существуют признаки того, что процент смертности птичего гриппа мог быть ниже, так как очень много людей со средней степенью тяжести симптомов не обращались за медицинской помощью и не были учтены в статистике.
В одном из случаев у мальчика с H5N1 первым симптомом была диарея; через короткий промежуток времени последовала кома. Респираторные симптомы подобные гриппу отсутствовали.
Были проведены исследования уровня цитокинов у людей, заражённых вирусом гриппа H5N1. В частности, беспокойство вызывал фактор некроза опухоли — белок связанный с разрушением тканей в областях инфекции, и увеличении выработки других цитокинов. Вызванное вирусом гриппа увеличение уровня цитокинов так же связано с симптомами, включающими лихорадку, озноб, рвоту и головные боли. Повреждение тканей связанных с патогенным вирусом гриппа может привести к смерти.
Каскад воспалительных процессов, вызванный H5N1 был назван некоторыми специалистами «цитокинным штормом» из-за того, что иммунная стимуляции, видимо, вызывает процесс положительной обратной связи, наносящий вред организму. H5N1 стимулирует большее увеличение уровня цитокинов, чем большинство вирусов гриппа.
См. также
- ООН Организация Объединенных Наций
- ВОЗ Всемирная Организация Здравоохранения
- The United Nation’s World Health Organization’s Avian Flu Facts Sheet for 2006 (недоступная ссылка). Архивировано 14 июля 2006 года.
- Epidemic and Pandemic Alert and Response. Архивировано 30 ноября 2012 года. Guide to WHO’s H5N1 pages
- Avian Influenza Resources (updated). Архивировано 30 ноября 2012 года. — tracks human cases and deaths
- National Influenza Pandemic Plans (недоступная ссылка). Архивировано 27 апреля 2005 года.
- WHO Collaborating Centres and Reference Laboratories (недоступная ссылка). Архивировано 26 декабря 2003 года. Centers, names, locations, and phone numbers
-
FAO Avian Influenza portal. Архивировано 30 ноября 2012 года. Information resources, animations, videos, photos
- FAO (недоступная ссылка). Архивировано 11 мая 2006 года. Food and Agriculture Organisation — Bi-weekly Avian Influenza Maps — tracks animal cases and deaths
- FAO Bird Flu disease card (недоступная ссылка). Архивировано 16 марта 2005 года.
- FAO Socio-Economic impact of AI (недоступная ссылка). Архивировано 23 сентября 2006 года. Projects, Information resources
- ВОЗ Всемирная Организация Здравоохранения
- OIE World Organisation for Animal Health — tracks animal cases and deaths
- Official outbreak reports by country. Архивировано 30 ноября 2012 года.
- Official outbreak reports by week (недоступная ссылка). Архивировано 27 сентября 2006 года.
- Chart of outbreaks by country. Архивировано 30 ноября 2012 года.
- Official — США
- PandemicFlu.Gov. Архивировано 30 ноября 2012 года. U.S. Government’s avian flu information site
- USAID (недоступная ссылка). Архивировано 27 мая 2005 года. U.S. Agency for International Development — Avian Influenza Response
- CDC. Архивировано 30 ноября 2012 года. Centers for Disease Control — responsible agency for avian influenza in humans in US — Facts About Avian Influenza (Bird Flu) and Avian Influenza A (H5N1) Virus
- USGS — NWHC. Архивировано 30 ноября 2012 года. National Wildlife Health Center — responsible agency for avian influenza in animals in US
- HHS. Архивировано 30 ноября 2012 года. U.S. Department of Health & Human Services — Pandemic Influenza Plan
- Official — Великобритания
- Exotic Animal Disease Generic Contingency Plan. Архивировано 30 ноября 2012 года. — DEFRA generic contingency plan for controlling and eradicating an outbreak of an exotic animal disease. PDF hosted by BBC (a government entity).
- UK Influenza Pandemic Contingency Plan. Архивировано 30 ноября 2012 года. — NHS (a government entity). Contingency planning for an influenza pandemic. PDF hosted by BBC
- Technical
External links dealing with technical aspects can be found here.
- News and General information
External links dealing with news and general information can be found here.